近日,我院肝脏肿瘤多学科团队首席专家、肝外科主任王鲁教授领衔研究团队发布了一项历时3年,以“患者来源类器官(PDOs)”为模型,发现了造成胆管癌患者化疗耐药的“元凶”,并开展靶向代谢联合化疗的动物实验。数据显示,这种创新联合疗法能使耐药肿瘤体积缩小50%以上,生存期大幅延长。该研究为未来提升胆管癌治疗疗效、突破耐药“瓶颈”提供了新方向。
国际期刊《Cancer Letters》上发表了这项重要研究成果。王鲁教授,王龙蓉教授和林镇海教授为该研究通讯作者。单季军博士和陈志文博士为共同第一作者,该文章影响因子为10.1分。

肝内胆管癌致死率高,化疗耐药成治疗瓶颈
肝内胆管癌是我国常见的原发性肝癌类型之一,发病率逐年上升。在我国发病率从1990年的1.4/10万到现在的6.3 /10万。
据悉,肝内胆管癌是一种症状隐匿且高度侵袭性的致死性疾病,多数患者确诊时已是中晚期,失去手术机会、5年生存率低。临床中,以吉西他滨联合顺铂或奥沙利铂的化疗方案,整体疗效不佳,患者中位总生存期约为9.5~9.7个月,部分患者对化疗药物出现天然或获得性耐药,严重影响治疗效果与生存期。
王鲁教授介绍说,化疗耐药是导致疗效不佳的核心原因。“临床上急需寻找新的治疗突破口,特别是采用提升化疗敏感性的精准策略,以此提高肝内胆管癌患者的。”王鲁教授强调。
研究揭示“代谢密码”,找到化疗耐药“元凶”
王鲁教授领衔团队以“患者来源类器官(PDOs)”为模型,模拟患者体内肿瘤真实状态,系统评估化疗响应差异。历时3年之后,他们发现,产生化疗耐药患者的肿瘤中存在明显的“脂肪酸代谢活跃”特征,这一代谢通路可能成为癌细胞逃避药物杀灭癌细胞的“拦路虎”。
据了解,研究团队通过18例胆管癌患者来源类器官(PDOs)模型和多组学分析,首次发现发生耐药的“元凶”是SUMO蛋白酶SENP3在耐药肿瘤中显著低表达,且与患者不良预后相关。
团队进一步研究后发现,甲基转移酶METTL3通过m6A修饰降解SENP3 mRNA,激活HADHA蛋白介导的脂肪酸氧化。“通过研究首次揭示胆管癌化疗耐药的关键机制——SENP3-HADHA代谢轴调控脂肪酸氧化(FAO)”王鲁教授说,在找到耐药机制和“元凶”后,我们提出了可以通过代谢联合化疗的新思路设计方案,逆转耐药性的发生比例。
"肿瘤细胞通过脂肪酸氧化疯狂'吸油'获取能量,像穿了防弹衣般抵抗化疗。而SENP3就是拆除这件防弹衣的关键开关。"第一作者单季军进一步解释道。
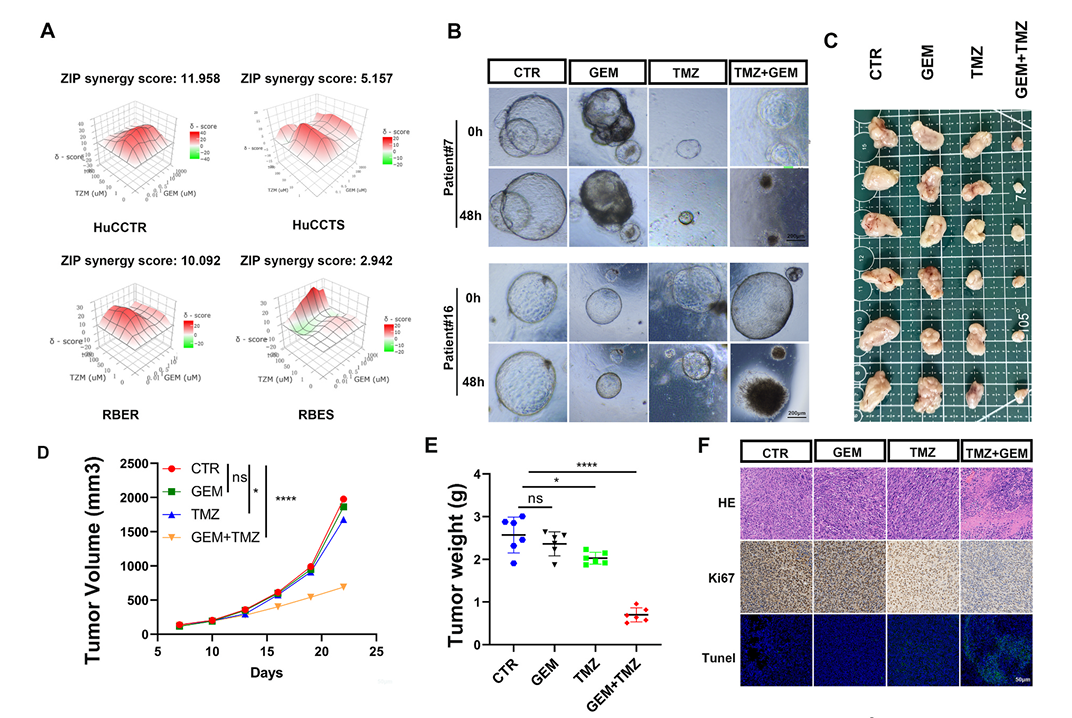
动物实验采用新方案,显著提升疗效破解耐药
在动物实验模型中,研究团队采用了“吉西他滨联合曲美他嗪”代谢联合靶向的方案。结果显示,这一创新联合治疗方案,不仅显著抑制肿瘤生长、延缓疾病进展。更令人鼓舞的是,这一方案在维持治疗安全性的同时,展现出良好的“器官保护”和“能量打击”双重作用,为临床治疗提供了新思路。
该研究首次揭示SENP3通过去SUMO化修饰调控HADHA蛋白稳定性,并阻断USP10介导的HADHA去泛素化,形成"SUMO-泛素化"双向调控网络。
"这相当于同时切断肿瘤的能量供应线和防御系统。"共同通讯作者林镇海教授强调,"该策略尤其适用于对传统化疗无效的耐药患者。"
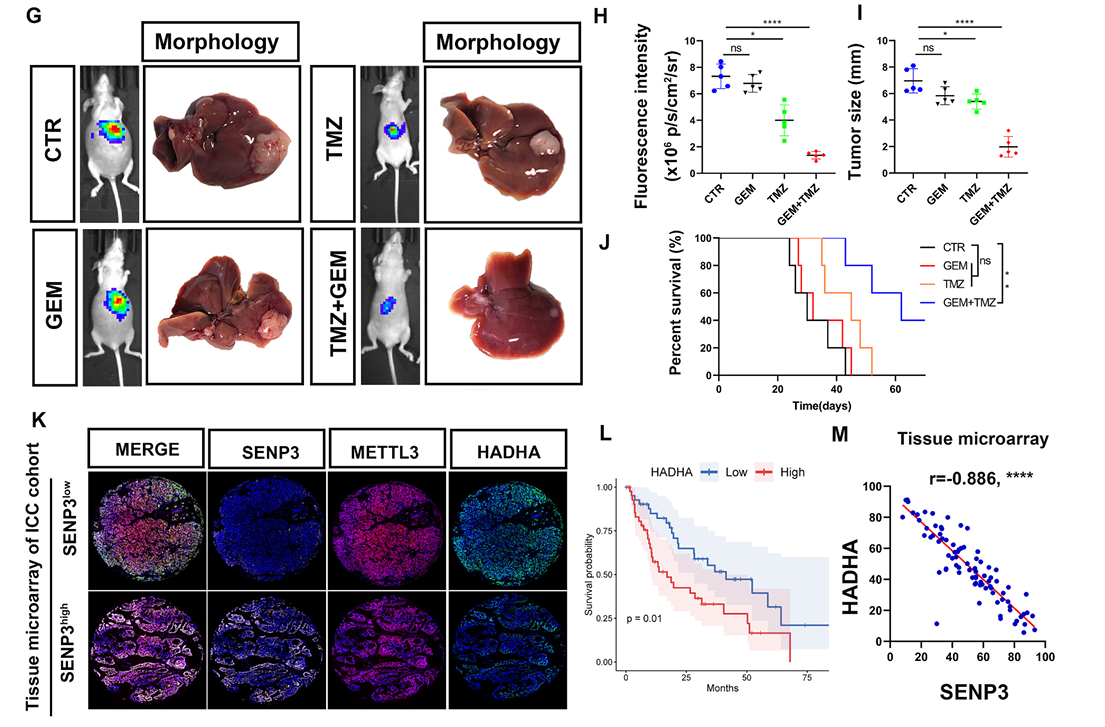
从实验室到临床应用,布局临床研究加速落地
“这是国际上首次揭示SENP3通过调控脂代谢机制影响胆管癌化疗效果的研究。”研究成员王龙蓉教授表示,“相关机制不仅揭开了胆管癌耐药的代谢本质,也为制定‘化疗+代谢抑制’组合策略提供了坚实理论支持。”
从实验室的可喜发现和突破,到临床应用还有多少路要走呢?
我院肝外科副主任赵一鸣教授指出:“从基础机制到动物实验证实,我们初步建立了SENP3-HADHA代谢轴在胆管癌治疗中的重要地位,下一步将推进临床研究,为更多胆管癌患者争取生存获益。”
目前,研究团队正积极推进相关临床转化工作,探索以SENP3表达为生物标志物,开展分型治疗和个体化方案设计。未来,化疗联合代谢抑制策略有望成为提升胆管癌治疗水平的新突破口。